Mengenal Partikel dan Notasi Atom
-1.jpg)
RG Squad, coba kamu bayangkan ada sebuah pensil yang dipotong hingga bagian terkecil. Maka, kamu bisa menyebutnya dengan atom. Wah, apa itu? Pengertian atom ialah partikel terkecil dari suatu materi hidup/tidak hidup. Contoh materi dalam kasus ini yaitu pensil, yang mempunyai ruang dan massa. Intinya, semua materi pasti tersusun atas kumpulan atom. Nah, untuk penjelasan lebih lanjut mengenai atom dan notasi atom (lambang), simak artikel berikut ya!
Atom dicetuskan pertama kali oleh seorang filsuf Yunani bernama Democritus bersama gurunya Leucippus pada tahun 400-an SM. Menurutnya atom berasal dari dua kata a berarti tidak dan tomos artinya tidak dapat dibagi lagi. Bentuknya dapat diibaratkan seperti sebuah bola dan terdiri dari 2 bagian yaitu:
- Inti atom/nukleus terdiri atas partikel bermuatan positif (proton) dan partikel tidak bermuatan (neutron).
- Kulit atom diisi oleh partikel negatif (elektron).
Kalau kamu bingung membayangkan komponen-komponennya, coba bayangkan tata surya yang berpusat pada matahari. Jadi, matahari inilah inti atom yang di dalamnya ada proton dan neutron. Sedangkan, orbit di sekitar matahari merupakan kulit dan planet-planetnya yang merupakan elektron.
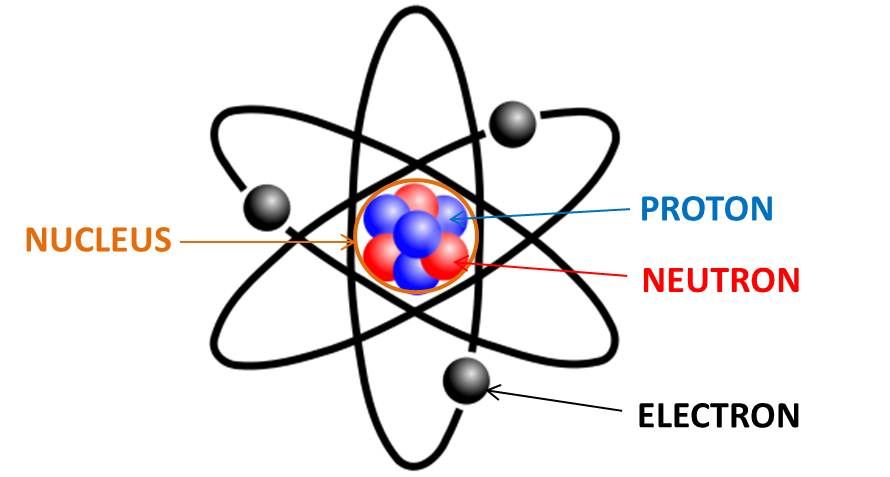
(Sumber: whoinventedfirst.com)
Setelah memahami konsep di atas, sekarang mari kita hitung berapa banyak jumlah proton, elektron, dan neutron jika diketahui notasi dari suatu unsur? Perhatikan baik-baik gambar di bawah ini:
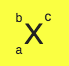
X: Simbol dari unsur
a: Nomor atom merupakan jumlah proton. Saat netral (tidak bermuatan) akan sama dengan jumlah elektron.
b: Nomor massa melambangkan jumlah proton ditambah jumlah neutron atau disebut juga jumlah nukleon.
c: Muatan/bilangan oksidasi (biloks) terdiri dari melepas elektron (positif) dan menangkap elektron atau bertambah (negatif).

Keterangan:
proton = 11
elektron = 11 (karena sama dengan proton yang netral/tidak bermuatan)
massa = 23
neutron = massa – proton
= 12
Pembahasan di atas merupakan contoh proton netral. Bagaimana jika bermuatan atau yang disebut dengan ion?
Kita coba dengan ion positif ya! Artinya melepas elektron.
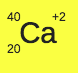
Keterangan:
proton = 20
elektron = 20 – 2 = 18 (karena muatan positif berarti elektron dilepas ya)
neutron = 40 – 20 =20
Sekarang, kita bahas ion negatif ya!
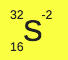
Keterangan:
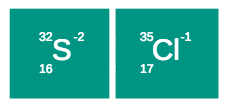
proton = 16
elektron = 16 + 2 = 18 (karena menangkap 2 elektron)
neutron = 32 – 16 = 16
Lalu, setelah kita membahas partikel-partikel tersebut, apa ya kesamaannya? Karena walau mereka berbeda-beda, ada kemungkinan atom penyusunnya sama. Berikut kesamaan partikel subatomik, kamu juga bisa corat-coret di kertas ya untuk membuktikannya:
- Isotop: nomor atomnya sama (proton) dan nomor massanya berbeda (neutron). Mudahnya, angka di bagian bawah sama sedangkan angka di bagian atas berbeda. Contoh:

- Isoton: neutronnya sama, tetapi nomor atom dan nomor massa berbeda. Mudahnya, selisih angka di atas dan bawah pasti sama.

- Isoelektron: elektronnya sama, tetapi nomor massa dan nomor atomnya berbeda. Biasanya terjadi pada ion.
- Isobar: nomor massanya sama, namun nomor atomnya beda. Cara mengingatnya, angka di bagian atas sama, sedangkan angka bagian bawahnya beda.

Okay Squad, sampai di sini dahulu penjelasannya. Jangan lupa dicoba-coba lagi ya di rumah untuk menghitung notasi atom. Oh ya, kalau kamu mau belajar lagi plus tanpa kuota, yuk coba pakai Ruangguru OTG dan dapatkan di toko buku Gramedia di kotamu!
















