Apa yang Dimaksud dengan Ikatan Ion? | Kimia Kelas 10
.jpg)
Sering ‘kan kamu mendengar iklan dengan kata-kata “Go Ion!”? Nah, apa kamu tahu apa maksudnya? Bagaimana pula bisa terjadi adanya ikatan ion dan pembentukannya? Jika kalian masih bingung dan belum memahaminya, mari simak sama-sama ya penjelasan di bawah ini. Baca baik-baik ya!
—
1. Pengertian
Ikatan ion terjadi akibat adanya serah terima elektron sehingga membentuk ion positif dan ion negatif yang konfigurasi elektronnya sama dengan gas mulia. Ion positif dan ion negatif diikat oleh suatu gaya elektrostatik. Senyawa yang dihasilkan disebut senyawa ion. Salah satu contoh yang sering kita jumpai sehari-hari adalah garam dapur.
Nah, garam dapur itu rumus kimianya adalah NaCl (Natrium klorida). Dalam NaCl padat terdapat ikatan antara ion Na+ dan ion Cl– dengan gaya elektrostatik, sehingga disebut ikatan ion. Bentuk kristal NaCl merupakan rangkaian antara ion Na+ dan ion Cl–. Satu ion Na+ dikelilingi oleh enam ion Cl– dan satu ion Cl– dikelilingi oleh enam ion Na+ seperti yang diilustrasikan oleh gambar di bawah.
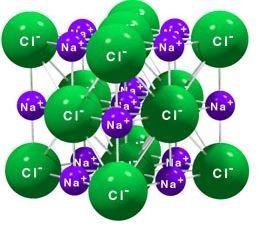
Gambar Struktur NaCl (1 Cl dikelilingi 6 Na dan sebaliknya 1 Na dikelilingi 6 Cl)
Baca juga: Mengenal Massa Molekul Relatif
2. Pembentukan
Seperti yang telah dibahas pada kaidah oktet sebelumnya, setiap unsur harus berusaha memiliki konfigurasi elektron seperti gas mulia, bisa dengan melepaskan elektron ataupun menerima elektron, supaya stabil. Peristiwa serah terima elektron ini terjadi pada senyawa NaCl alias garam dapur.
Bagaimana ceritanya? Na merupakan golongan IA dimana IA memiliki elektron valensi 1, sehingga supaya stabil IA harus melepas 1 elektron. Kalo dilihat dari konfigurasi elektronnya, 11Na: 2, 8, 1. Sehingga ketika melepas 1 elektron, maka elektron paling terakhinya menjadi 8 (sesuai kaidah oktet). Karena melepas 1 elektron, maka Na yang asalnya netral berubah menjadi bermuatan +1 (Na+). Reaksinya:
Na → Na+ + e- (artinya Na melepas 1 elektron, lihat elektron berada di sebelah kiri panah)
Oke, sekarang kira-kira ke mana tuh 1 elektron tadi yang dilepas Na? Hilang? Tidak, di sana ada yang menangkapnya yaitu si Cl. Kenapa bisa? Karena Cl memiliki elektron valensi 7 (dia golongan VIIA). Ya kalau dilihat dari konfigurasi elektronnya 17Cl : 2, 8, 7. Jadi kalau Cl menangkap 1 elektron, konfigurasinya menjadi 2, 8, 8, dengan elektron terakhirnya 8, ini sudah mematuhi kaidah oktet. Karena Cl menangkap 1 elektron maka Cl yang asalnya netral berubah menjadi -1 (Cl–). Reaksinya:
Cl + e- → Cl- (artinya Cl menerima 1 elektron, lihat elektron berada di sebelah kiri panah
Nah sekarang, apa pengaruhnya pembentukan Na+ dan Cl– ini? Sesuai Hukum Coulomb, muatan yang berbeda jenis akan saling tarik menarik. Sehingga Na+ ini akan berikatan dengan Cl– dengan gaya elektrostatik.
Na+ + Cl– → NaCl
Untuk lebih jelasnya perhatikan gambar berikut:
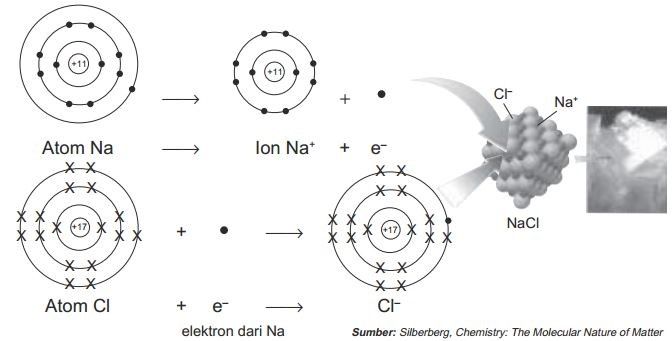
Proses pembentukan ikatan ion pada NaCl
Kira-kira unsur apa saja yang bisa membentuknya?
Ikatan ion = logam + nonlogam
Kalo digeneralisir, ikatan logam itu diantaranya Golongan IA (kecuali H), IIA (kecuali Be), IIIA (Aluminium), golongan transisi (Golongan B). Sedangkan nonlogam, diantaranya golongan IVA-VIIA, kalau VIIIA relatif stabil.
.png)
Sekarang pastinya kalian sudah paham dong pengertian dan bagaimana proses pembentukannya? Kalian harus memahami rumus-rumusnya terlebih dahulu ya! Ketika rumus sudah dikuasai, pasti akan mudah untuk mengerjakan soal-soal. Nah, gabung di ruangbelajar untuk belajar yang lebih optimal bersama ahlinya.
![[AB] Web Side Banner - Blog RG](https://cdn-web-2.ruangguru.com/landing-pages/assets/399009fa-feaf-4b6c-8321-92409d53a26a.png)














