Klasifikasi Sistem Periodik Unsur Kimia & Cara Membacanya | Kimia Kelas 10
Apa itu sistem periodik unsur pada ilmu kimia? Yuk, kita pelajari mulai dari pengertian, gambar, manfaat, klasifikasi, serta cara membacanya di artikel Kimia kelas 10 ini!
—
Pernahkah kamu melihat tabel periodik kimia yang biasa ditempel di perpustakaan atau di dinding laboratorium kimia? Yap betul, yang bentuknya kotak-kotak kayak game tetris itu, hehe. Kamu tahu nggak sih, tabel itu maksudnya apa? Biar nggak penasaran, yuk kita bahas selengkapnya!
Apa Itu Sistem Periodik Unsur?
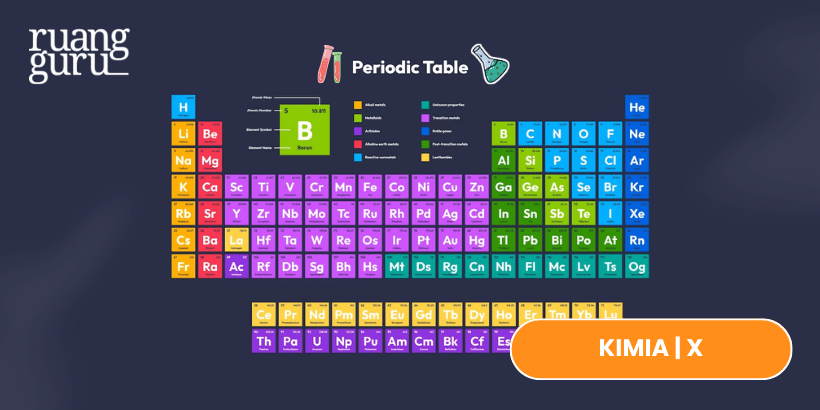
Sistem periodik unsur adalah suatu bentuk tabel yang berisi susunan unsur-unsur kimia berdasarkan nomor atom yang dimiliki. Karena berbentuk tabel, maka sistem ini disebut juga sebagai tabel periodik unsur atau tabel periodik kimia. Kamu dapat melihat gambar sistem periodik pada infografik berikut.
Sistem periodik unsur yang terdiri dari golongan dan periode (Lajur vertikal disebut GOLONGAN, Lajur horizontal disebut PERIODE) (Sumber: kuttabku.com)
Tabel ini merupakan rumusan grafik dari hukum periodik yang menyatakan bahwa sifat-sifat unsur kimia menunjukkan ketergantungan periodik pada nomor atom yang dimiliki masing-masing unsur. Tabel ini dibagi menjadi empat area persegi panjang yang disebut sebagai blok.
Nah, tahukah kamu kalau unsur-unsur dalam sistem periodik unsur kimia terdiri dari dua kelompok. Pertama yaitu golongan, dan kedua adalah periode. Baris-baris pada tabel disebut sebagai periode, sedangkan kolom-kolomnya disebut sebagai golongan. Unsur-unsur dari golongan yang sama pada sistem periodik menunjukkan karakteristik kimia yang serupa.
Selain itu, terdapat pula dua cara penamaannya dengan cara tradisional dan IUPAC (International Union of Pure and Applied Chemistry). Pada tingkat SMA ini, akan dibahas pengelompokkan unsur cara tradisional, nih. Pada konsep ini, nomor golongan lebih erat hubungannya dengan konfigurasi elektron dibandingkan cara IUPAC.
Baca Juga: Mengenal Macam-Macam Sifat dan Unsur Gas Mulia
Apa Saja yang Ada di Dalam Sistem Periodik?
Dalam sistem periodik, terdapat beberapa hal yang perlu kamu tahu, yaitu periode, golongan, dan blok. Yuk, kita bahas satu per satu!
a. Periode
Periode merupakan sebutan bagi lajur horizontal dalam sistem periodik unsur kimia. Periode suatu unsur menunjukkan nomor kulit yang sudah terisi elektron (n terbesar) berdasarkan konfigurasi elektron. Dalam sistem periodik unsur terdapat 7 periode, yaitu:
- Periode ke-1: terdiri atas 2 unsur.
- Periode ke-2: terdiri atas 8 unsur.
- Periode ke-3: terdiri atas 8 unsur.
- Periode ke-4: terdiri atas 18 unsur.
- Periode ke-5: terdiri atas 18 unsur.
- Periode ke-6: terdiri atas 32 unsur, yaitu 18 unsur seperti pada periode ke-4 atau ke-5, dan 14 unsur lagi merupakan deret lantanida.
- Periode ke-7: merupakan periode unsur yang belum lengkap. Pada periode ini terdapat deret aktinida.
b. Golongan
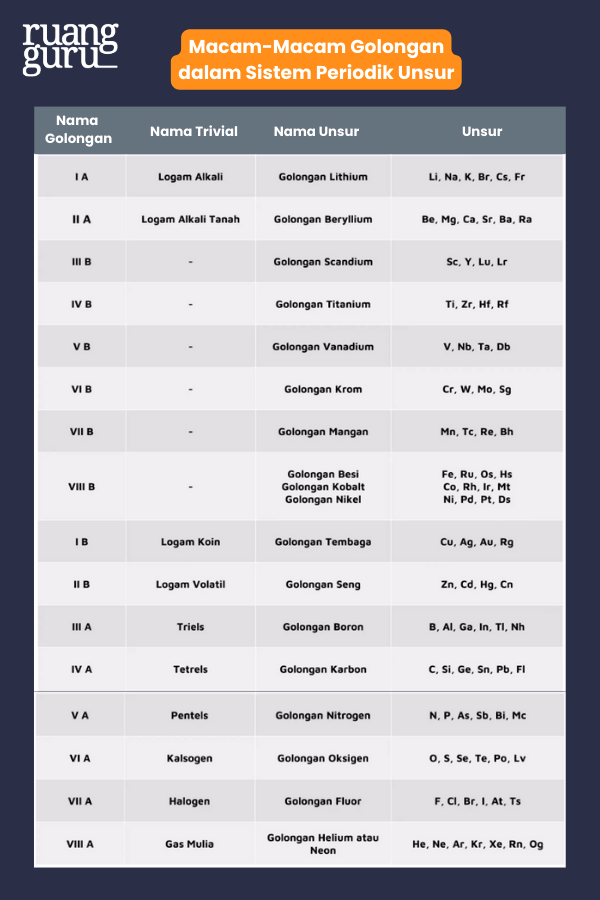
Golongan merupakan sebutan bagi lajur vertikal dalam sistem periodik unsur modern. Penentuan golongan berkaitan dengan sifat-sifat yang dimiliki unsur tersebut. Unsur-unsur dalam satu golongan memiliki sifat-sifat yang mirip. Beberapa golongan diberi nama khusus, yaitu:
- Golongan IA disebut golongan alkali (kecuali H), yang terdiri dari H (Golongan IA tetapi bukan alkali), Li, Na, K, Rb, Cs, Fr.
- Golongan IIA disebut golongan alkali tanah, yang terdiri dari Be, Mg, Ca, Sr, Ba, Ra.
- Golongan VIIA disebut golongan halogen, yang terdiri dari F, Cl, Br, I, At.
- Golongan VIIIA disebut gas mulia, yang terdiri dari He, Ne, Ar, Kr, Xe, Rn.
- Golongan IIIA disebut golongan boron-aluminium, yang terdiri dari B, Al, Ga, In, Ti.
- Golongan IVA disebut golongan karbon-silikon, yang terdiri dari C, Si, Ge, Sn, Pb.
- Golongan VA disebut golongan nitrogen-fosforus, vang terdiri dari N, P, As, Sb, Bi.
- Golongan VIA disebut golongan oksigen-belerang, yang terdiri dari O, S, Se, Te, Po.
- Golongan IB sampai dengan VIIIB disebut golongan transisi.
c. Blok
Blok tabel periodik adalah kumpulan unsur yang disatukan oleh orbital atom dari elektron valensi atau kekosongannya. Blok terbagi menjadi empat bagian, yaitu blok s, p, d, dan f. Berikut penjelasan selengkapnya mengenai masing-masing blok.
1. Blok s
Blok s berada di sebelah kiri tabel periodik standar dan terdiri atas unsur-unsur dari dua kolom pertama ditambah satu unsur di kolom paling kanan, nonlogam hidrogen dan helium, logam alkali (dalam golongan 1), serta logam alkali tanah (golongan 2). Konfigurasi elektron umum unsur blok s adalah nsˆ(1–2).
2. Blok p
Blok p berada di sebelah kanan tabel periodik standar dan mencakup unsur-unsur dalam golongan 13 sampai 18. Konfigurasi elektron umum unsur blok p adalah nsˆ2 npˆ(1–6).
3. Blok d
Blok d berada di tengah tabel periodik dan mencakup unsur-unsur dari golongan 3 sampai 12, dimulai pada periode ke-4. Semua unsur kimia pada blok d juga dikenal sebagai logam transisi karena mereka menempati zona transisi dalam sifat, antara logam yang sangat elektropositif dari golongan 1 dan 2, serta logam yang elektropositif lemah dari golongan 13 sampai 16.
4. Blok f
Blok f merupakan blok yang terdiri atas unsur pada periode mulai dari yang keenam dan seterusnya. Unsur-unsur ini terkadang disebut sebagai logam transisi dalam karena mereka menyediakan transisi antara blok s dan blok d pada baris (periode) ke-6 dan ke-7, dengan cara yang sama seperti logam transisi blok d menyediakan jembatan transisi antara blok s dan blok p pada baris ke-4 dan ke-5.
Manfaat Sistem Periodik
Penyusunan sistem periodik memiliki beberapa manfaat, antara lain yaitu untuk mengetahui dan mengenal nama-nama unsur kimia, untuk mengetahui berat unsur atom, untuk mengetahui konfigurasi elektron unsur, serta untuk mengetahui jumlah unsur atom. Selain itu, adanya sistem periodik unsur juga dapat memudahkan siapapun yang ingin mempelajari lebih mendalam mengenai unsur-unsur kimia.
Klasifikasi Sistem Periodik
Unsur-unsur kimia memiliki pengelompokan berdasarkan sifat fisika dan kimianya sesuai gejala yang dialami oleh unsur tersebut. Oleh karena itu, terdapat beberapa klasifikasi sistem periodik yang perlu kamu tahu, antara lain yaitu:
a. Sifat-Sifat Umum
Secara umum, unsur-unsur kimia memiliki sifat fisika dan kimia yang terdiri atas tiga kategori, yaitu logam, nonlogam, dan metaloid. Logam biasanya berupa padatan yang berkilau dengan konduktivitas tinggi dan dapat membentuk alloy dengan bentuk logam lainnya untuk membentuk senyawa ion berupa garam dengan nonlogam atau selain gas mulia.
Baca Juga: Sifat Unsur Halogen dan Manfaatnya dalam Kehidupan Sehari-Hari
Sementara itu, nonlogam biasanya berbentuk gas berwarna atau tidak berwarna yang bisa membentuk senyawa dengan bentuk non logam lainnya secara kovalen. Sedangkan metaloid biasanya bersifat di antara logam dan nonlogam ataupun cempuran dari kedua unsurnya.
b. Keadaan Materi
Klasifikasi selanjutnya yaitu berdasarkan wujud materi atau fase unsur tersebut, seperti cair, padat, atau gas dalam temperatur dan tekanan standar (STP). Biasanya unsur yang berwujud padat akan memiliki temperatur konvensional dengan tekanan atmosfer. Sedangkan unsur yang berwujud cair hanya Brom dan Raksa pada 0°C atau sekitar 32°F dengan tekanan atmosfer normal.
c. Titik Lebur dan Titik Didih
Titik lebur dan titik didih digunakan untuk mendefinisikan karakter unsur yang dinyatakan dengan derajat celcius pada tekanan atmosfer tertentu. Sebenarnya, klasifikasi unsur berdasarkan titik lebur dan titik didih sudah diketahui, namun ada beberapa unsur radioaktif dengan jumlah sangat kecil yang belum diketahui.
Helium atau He hanya memiliki titik didih dan tidak memiliki titik lebur pada penyajian konvensional karena tetap berada pada wujud cair meskipun dalam keadaan nol mutlak pada tekanan atmosfer.
d. Massa Jenis
Klasifikasi tabel periodik juga seringkali menggunakan massa jenis pada temperatur dan tekanan standar (STP) sebagai karakter unsur kimia. Massa jenis biasanya juga dinyatakan untuk wujud gas pada temperatur pengukuran wujud tertentu. Misalnya, saat dicairkan atau dipadatkan, maka unsur gas akan memiliki massa jenis yang sama dengan unsur kimia lainnya.
e. Struktur Kristal
Unsur kimia yang diteliti sampai saat ini sebagai sampel zat padat memiliki delapan jenis struktur kristal dalam materialnya, yaitu kubik, kubik pusat badan, kubus pusat muka, heksagonal, monokinis, ortorombik, rhombohedral, dan tetragonal. Pada beberapa unsur transuranium sintetis, sampel unsur kimia yang tersedia sangat sedikit jumlahnya untuk bisa menentukan struktur kristalnya.
Baca Juga: Konsep Struktur Lewis dalam Ikatan Kovalen & Cara Menggambarnya
Cara Membaca Sistem Periodik
Terdapat beberapa cara untuk membaca tabel sistem periodik, antara lain yakni sebagai berikut:
1. Tabel sistem periodik kimia tersusun berdasarkan nomor atom, sehingga semakin ke kanan dan ke bawah, nomor atom akan semakin besar.
2. Setiap unsur kimia pasti mengandung 1 proton lebih banyak daripada atom di sebelah kirinya dalam tabel periodik.
3. Golongan tabel periodik ditampilkan oleh kolom vertikal dan golongan ini dicirikan dengan beberapa warna yang sama. Warna ini dapat digunakan untuk membantu mengidentifikasi unsur-unsur mana yang memiliki sifat fisik dan kimia yang hampir mirip.
4. Jika unsur kimia bertambah maka penggolongannya juga akan semakin sulit. Oleh karena itu, terdapat ruang kosong pada tabel sistem periodik kimia. Misalnya, pada 3 baris pertama tabel memiliki ruang kosong karena berfungsi untuk logam transisi yang akan dimunculkan di tabel periodik, yaitu nomor atom 21.
5. Semua unsur kimia pada satu periode pasti memiliki jumlah orbital atom yang sama, kemudian akan dilintasi oleh elektron-elektron tertentu. Jumlah orbital ini akan sesuai dengan jumlah periode pada tabel periodik dengan menunjukan 7 baris yang artinya adalah 7 periode. Misalnya, unsur periode 1 dengan 1 orbital, sedangkan unsur periode 7 juga memiliki 7 orbital. Contoh tersebut diberi nomor 1-7 dari atas ke bawah di bagian kiri tabel periodik.
—
Demikian penjelasan mengenai sistem periodik unsur kimia mulai dari pengertian, gambar, manfaat, klasifikasi, serta cara membacanya. Gimana? Udah mulai pusing, belum? Kalau kamu pusing dan butuh bantuan, angkat tangan kamu dan lambaikan ke arah kamera! Hehe, nggak deng canda! Kalau kamu butuh bantuan, yuk langsung aja join les privat kimia bersama Ruangguru Privat! Dijamin kamu nggak akan pusing lagi deh setiap kali belajar kimia!
Referensi:
https://id.wikipedia.org/wiki/Tabel_periodik (Diakses pada 28 Mei 2023)
https://id.wikipedia.org/wiki/Blok_tabel_periodik (Diakses pada 28 Mei 2023)
https://www.detik.com/edu/detikpedia/d-5856613/tabel-periodik-unsur-kimia-sejarah-fungsi-sifat-sifat-dan-gambarnya (Diakses pada 28 Mei 2023)
https://www.merdeka.com/jatim/sistem-periodik-unsur-kimia-kenali-sifat-sifat-dan-penomoran-di-dalamnya-kln.html (Diakses pada 28 Mei 2023)
https://kumparan.com/berita-update/tabel-periodik-unsur-ini-4-tujuannya-yang-perlu-diketahui-1uyD8qnd9rP/full (Diakses pada 28 Mei 2023)
Sumber Gambar:
https://www.freepik.com/free-vector/periodic-table-design-template_29760124.htm#query=periodic%20tabel&position=1&from_view=search&track=ais (Diakses pada 19 September 2023)
![[AB] Web Side Banner - Blog RG](https://cdn-web-2.ruangguru.com/landing-pages/assets/399009fa-feaf-4b6c-8321-92409d53a26a.png)














